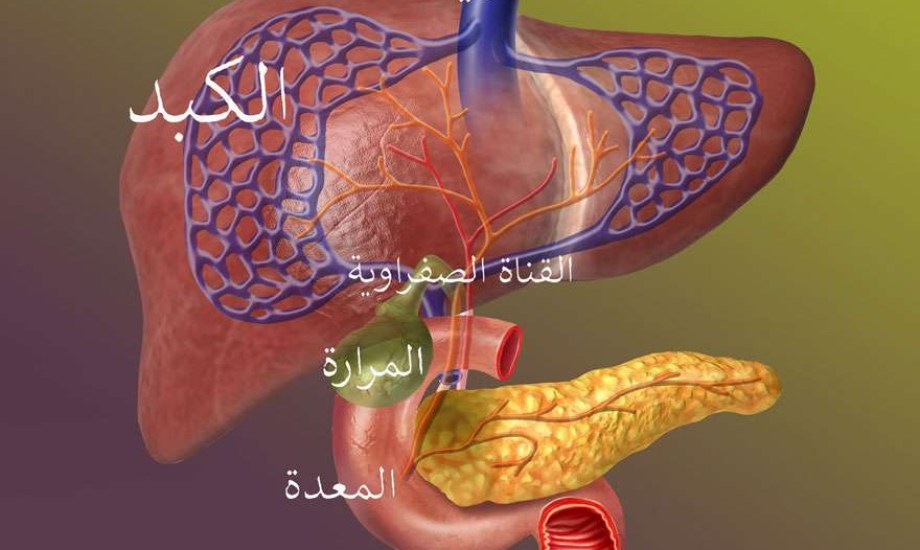
علاج ثوري للحكة الصفراوية يحصل على موافقة FDA
تُشكل الحكة المزمنة أحد أكثر الأعراض إزعاجاً لدى مرضى التهاب القنوات الصفراوية الأولي (PBC)، وهو مرض مناعي نادر يصيب الكبد ويؤثر على تدفق العصارة الصفراوية، ورغم أن هذا العرض قد يبدو بسيط ظاهرياً، إلا أنه في الواقع يمثل عبئاً كبيراً على المرضى؛ إذ قد يؤدي إلى اضطرابات النوم والإرهاق وتدهور جودة الحياة بشكل ملحوظ.
الحكة الصفراوية: عرض خفي وتأثير عميق
يعاني ما يصل إلى 89% من المرضى المصابين بـPBC من الحكة الصفراوية، وهي حكة داخلية لا يمكن تخفيفها بالحك التقليدي، ويُعتقد أن تراكم الأحماض الصفراوية في الدم نتيجة اضطراب تدفق الصفراء هو العامل الرئيسي وراء هذا الشعور المزعج.
هذه الحالة لا تقتصر على الإزعاج فقط، بل قد تتفاقم لتؤثر على الحياة اليومية حيث يعاني المرضى من الأرق المستمر والإجهاد، وقد يصل الأمر في بعض الحالات إلى الحاجة لزراعة الكبد حتى دون وجود فشل كبدي فعلي.
 عملية زراعة الكبد
عملية زراعة الكبد
دواء Lynavoy: خيار علاجي جديد
في خطوة مهمة، وافقت إدارة الغذاء والدواء الأمريكية (FDA) على دواء (Lynavoy)، ليكون أول علاج مخصص للحكة الصفراوية لدى هؤلاء المرضى. ينتمي الدواء إلى فئة مثبطات ناقل الأحماض الصفراوية في اللفائفي (IBAT) حيث يعمل على تقليل إعادة امتصاص الأحماض الصفراوية مما يؤدي إلى خفض مستوياتها في الدورة الدموية وبالتالي تقليل الإشارات المسببة للحكة، ويتميز Lynavoy بكونه علاج فموي موجّه يركز على السبب البيولوجي للحكة بدلاً من مجرد تخفيف الأعراض بشكل مؤقت.
أهمية الموافقة الدوائية
تمثل هذه الموافقة تحولاً مهماً في علاج الحكة المرتبطة بأمراض الكبد؛ خاصة أن الخيارات العلاجية السابقة كانت محدودة وغير فعالة في كثير من الحالات، كما يعكس ذلك توجه متزايد نحو تطوير علاجات تستهدف آليات المرض بشكل دقيق.
ولا تزال طلبات تسجيل الدواء قيد المراجعة في عدة مناطق، بما في ذلك الاتحاد الأوروبي والمملكة المتحدة وكندا والصين، ما يشير إلى إمكانية توفره عالمياً خلال الفترة المقبلة.
 دواء Lynavoy
دواء Lynavoy
دور الدراسة السريرية في دعم القرار
استندت الموافقة إلى نتائج دراسة (GLISTEN9 من المرحلة الثالثة والتي نُشرت بياناتها في 2024، حيث أظهرت تحسناً ملحوظاً وسريعاً في شدة الحكة مقارنة بالعلاج الوهمي.
وشملت الدراسة تصميم عشوائي مزدوج التعمية وحققت أهدافها الأساسية والثانوية؛ إذ بدأ التحسن في الأسبوع الثاني من العلاج واستمر لمدة 24 أسبوعاً، كما أظهرت النتائج تحسناً في اضطرابات النوم المرتبطة بالحكة.
وعلى مقياس رقمي من 0 إلى 10 لتقييم شدة الحكة سجل المرضى الذين تلقوا العلاج انخفاض ملحوظ مقارنة بالمجموعة الضابطة مع دلالة إحصائية قوية.
السلامة والآثار الجانبية
أظهرت البيانات أن الدواء يتمتع بملف أمان متوافق مع الدراسات السابقة، وكانت الآثار الجانبية الأكثر شيوعاً هي الإسهال وآلام البطن وغالباً ما كانت خفيفة إلى متوسطة الشدة، كما لوحظت نسبة منخفضة من إيقاف العلاج بسبب هذه الأعراض، مما يعزز من إمكانية استخدامه على نطاق واسع لدى المرضى.
أمل جديد لمرضى الأمراض النادرة
حصل الدواء على تصنيف "دواء يتيم" في الولايات المتحدة والاتحاد الأوروبي واليابان، وهو ما يعكس أهمية هذا العلاج لفئة محدودة من المرضى الذين يعانون من مرض نادر يفتقر إلى خيارات علاجية كافية.